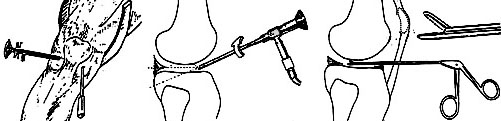
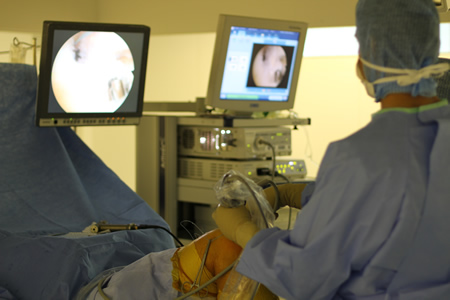
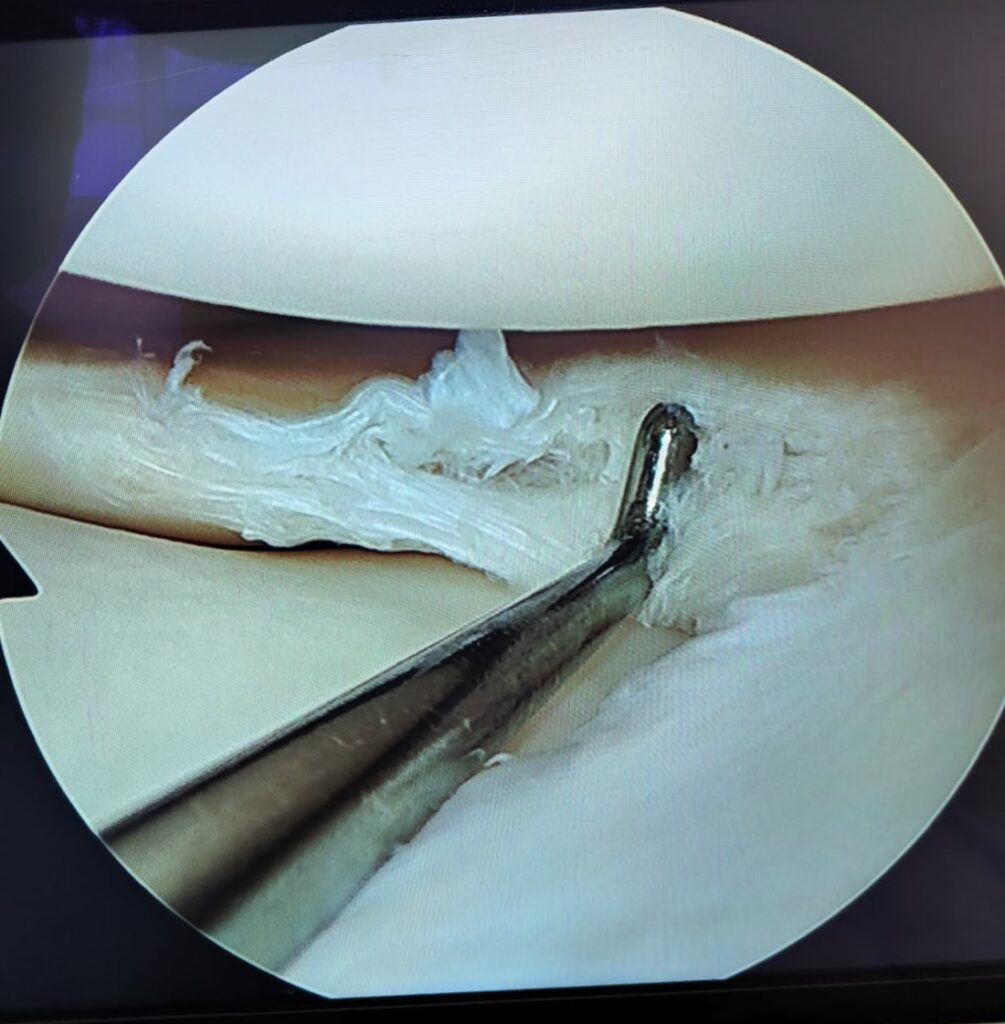
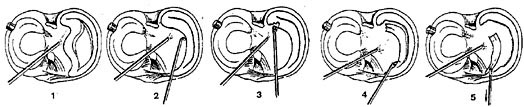
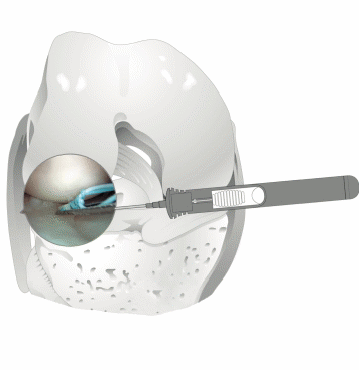
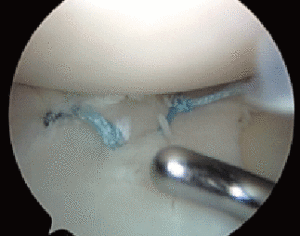
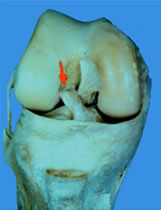
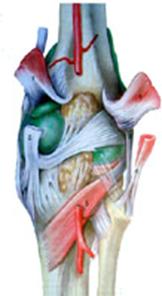
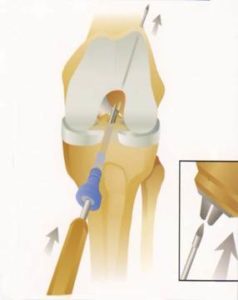
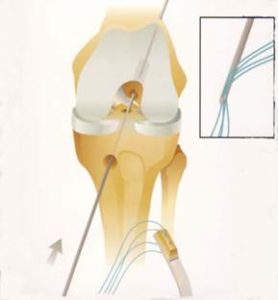
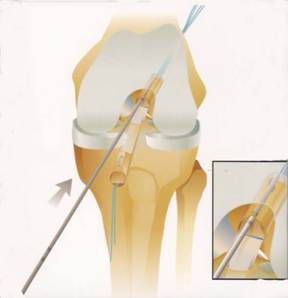
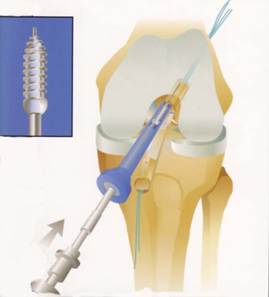
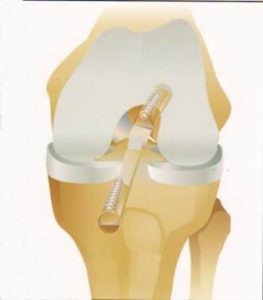
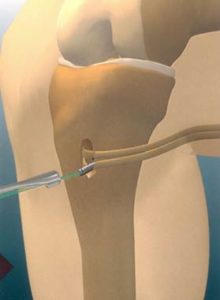
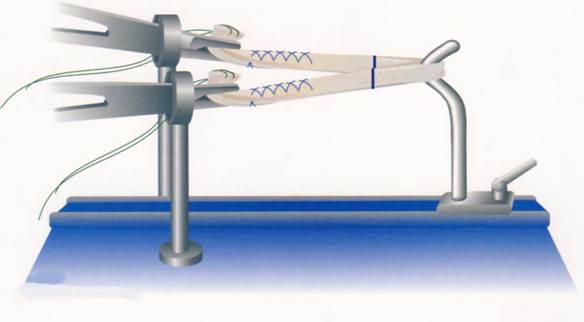
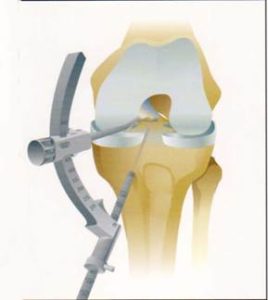
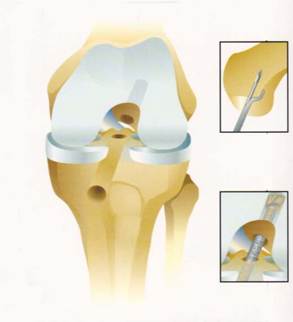
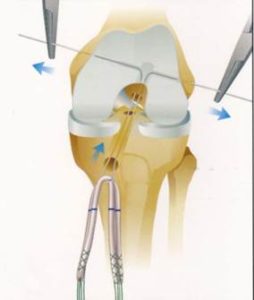
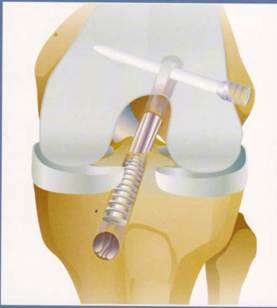
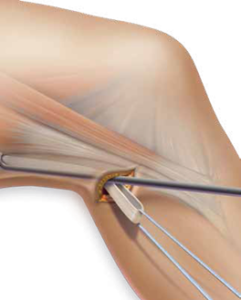
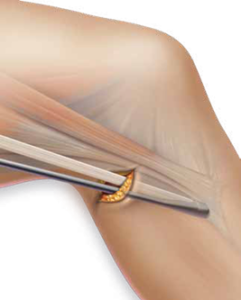
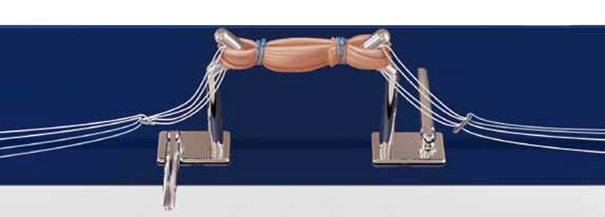
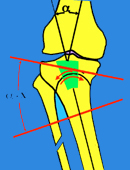
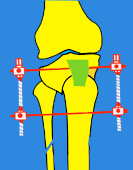
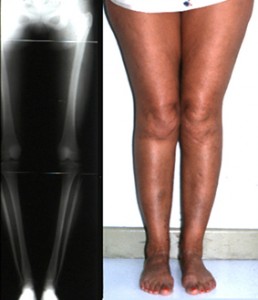
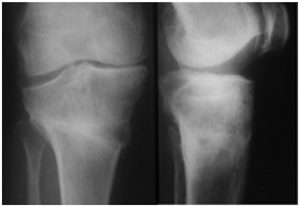
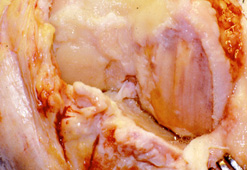
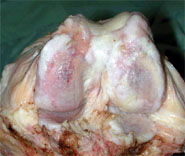
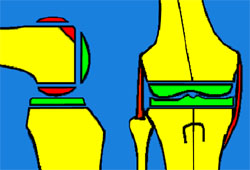
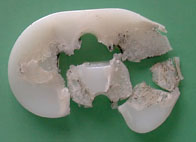
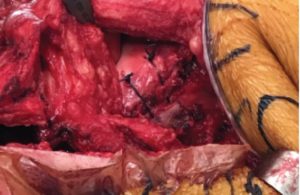
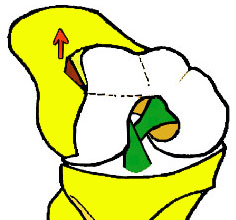
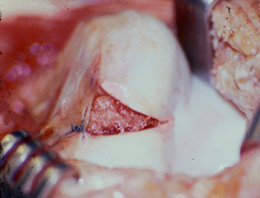
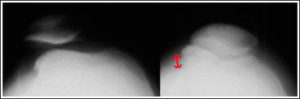
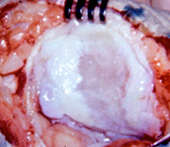
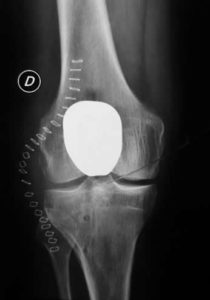
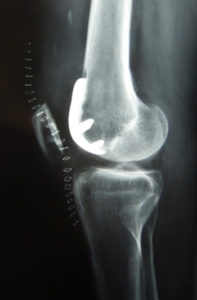
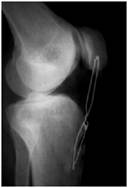
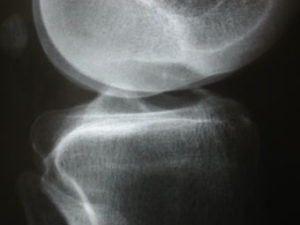
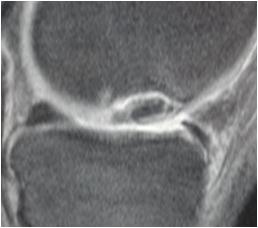
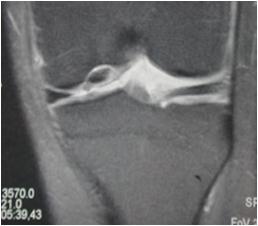
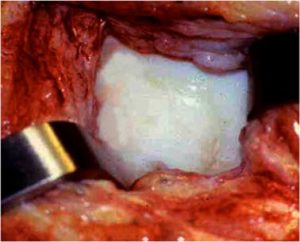
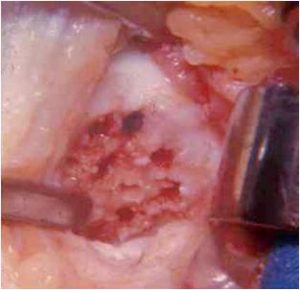
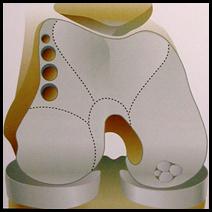
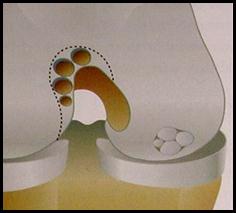
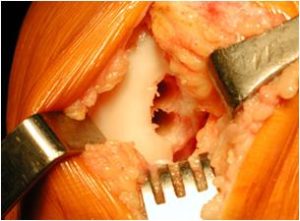
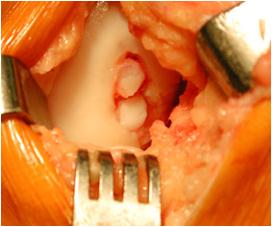
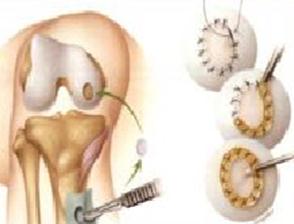
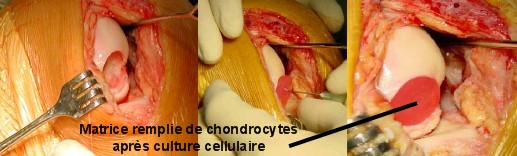
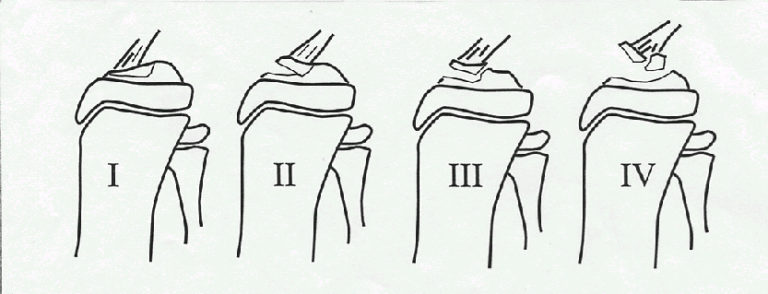
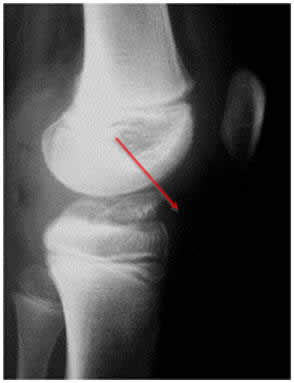
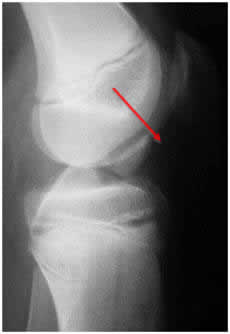
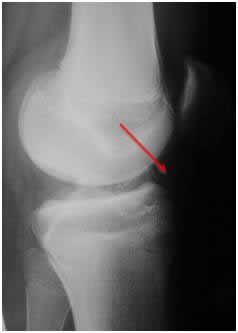
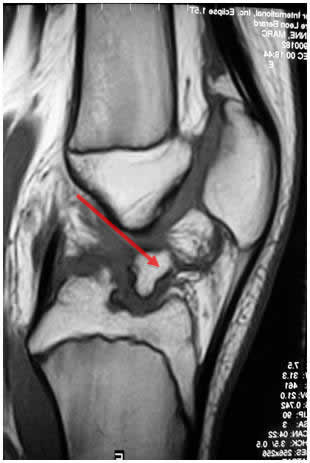
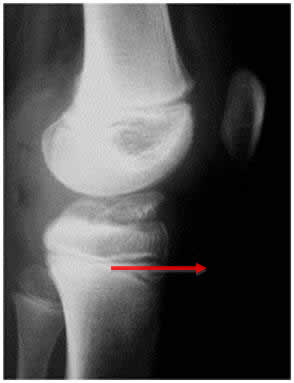
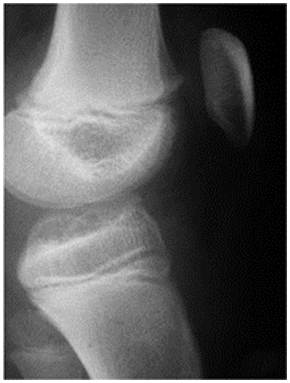
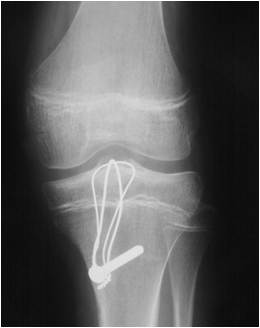
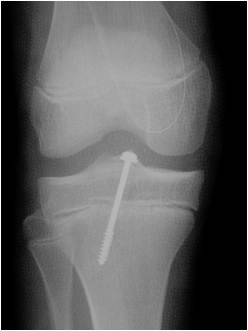
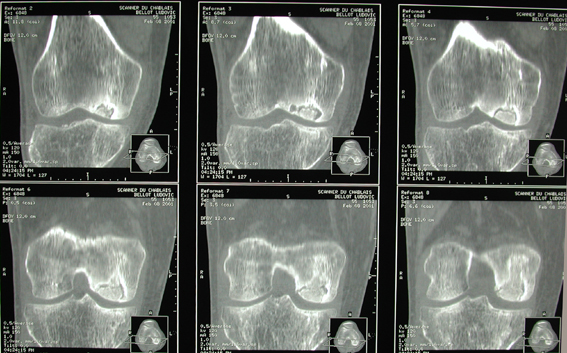
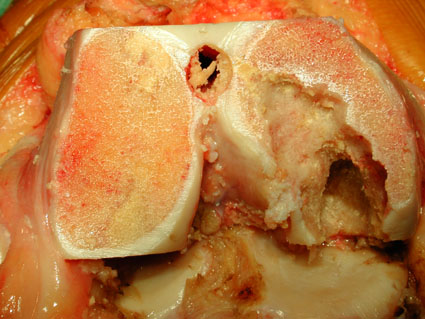
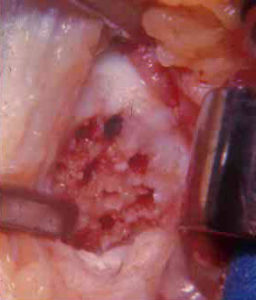
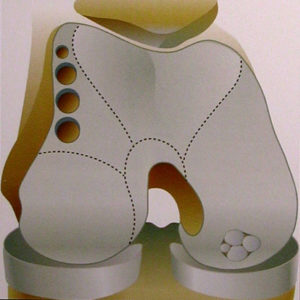
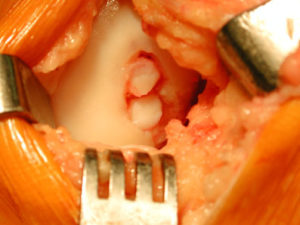
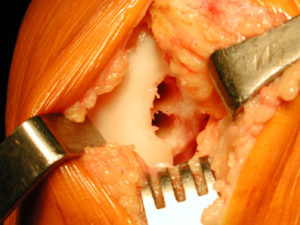
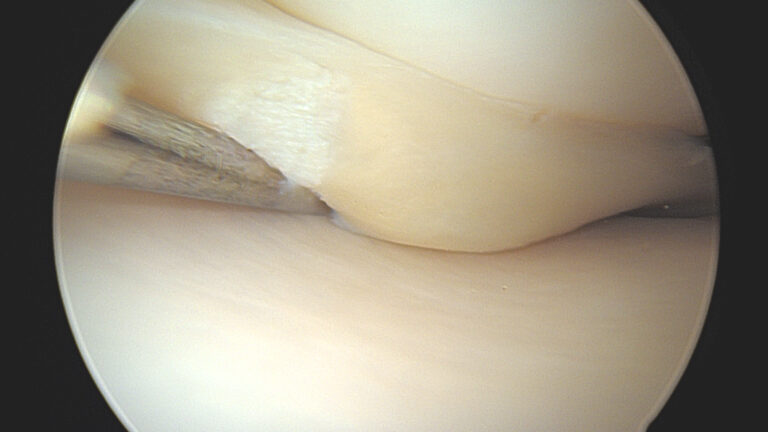
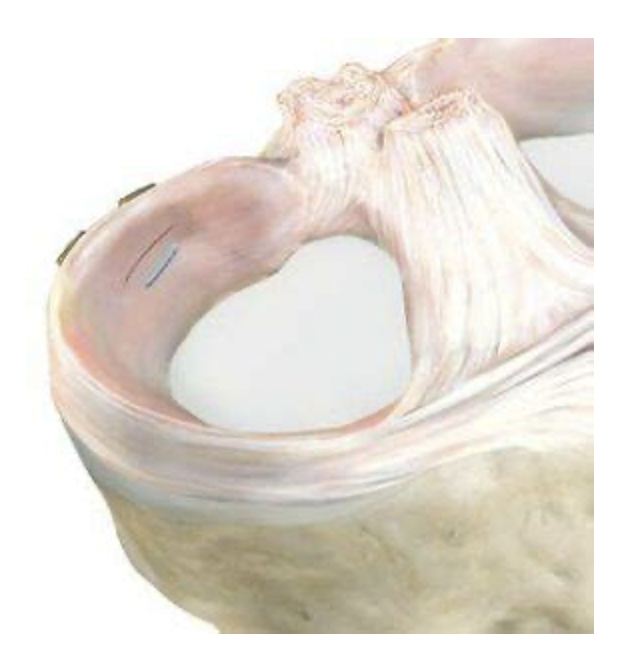
3. Suites opératoires et rééducation après réparation méniscale
- Réparation méniscale isolée
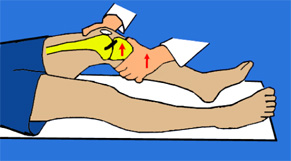
Dans ce cas le patient doit soulager l’appui par des cannes anglaises pendant 3 semaines. La première semaine il doit se mettre au repos et glacer régulièrement son genou. La kinésithérapie commencera 8 jours après l’intervention. On commencera par mobiliser le genou en ne dépassant pas 90° de flexion avant la fin de la 4è semaine. Les positions à genoux et accroupi sont interdite pendant les 3 mois qui suivent l’intervention. Ces 3 mois correspondent au délai moyen de cicatrisation méniscale.
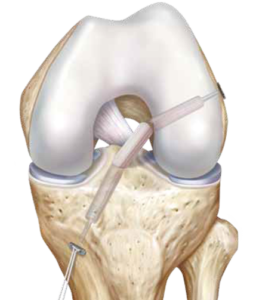
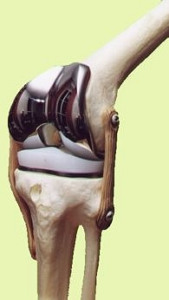
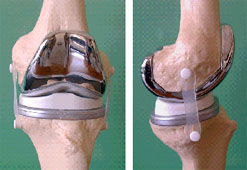
- Réparation méniscale associée à une ligamentoplastie du genou.
Le protocole de rééducation est le même que pour une ligamentoplastie isolée.
4. Résultats
Les résultats de ces réparations méniscales sont les suivants :
- 20% de méniscectomies secondaires
- 20% de douleurs résiduelles
- 60% de genoux totalement asymptomatiques
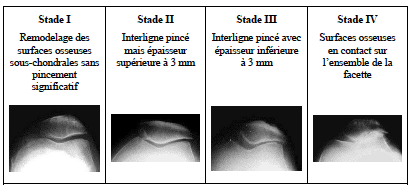
Mais à 10 ans de recul on ne retrouve que 10% de modification de l’interligne articulaire (signe l’apparition de l’arthrose) contre 28% lors des ménisectomies (régularisation méniscale) internes et 40% lors des ménisectomies (régularisation méniscale) externes.
Au total dès que les conditions sont réunies pour proposer une réparation du ménisque celle-ci doit être tentée en prévenant le patient des risques d’échec (20% soit 1 réparation sur 5).